
Мы сообщаем о кинетике иммунных реакций в отношении клинических и вирусологических особенностей пациента с легкой и умеренной коронавирусной болезнью 2019 года (COVID-19), который потребовал госпитализации. Увеличение клеток, секретирующих антитела (ASC), фолликулярных хелперных T-клеток (T FH- клеток), активированных CD4 + T-клеток и CD8 + T-клеток и антител иммуноглобулина M (IgM) и IgG, которые связывают вызывающий COVID-19 коронавирус SARS-CoV -2 были обнаружены в крови до симптоматического выздоровления. Эти иммунологические изменения сохранялись в течение не менее 7 дней после полного исчезновения симптомов.
47-летняя женщина из Ухани, провинция Хубэй, Китай, была представлена в отделение неотложной помощи в Мельбурне, Австралия. Симптомы у нее начались на 4 дня раньше: вялость, боль в горле, сухой кашель, плевритная боль в груди, легкая одышка и субъективная лихорадка (рис. 1а ). Она отправилась из Ухани в Австралию за 11 дней до презентации. Она не имела контактов с рынком морепродуктов Huanan или с известными случаями COVID-19. В остальном она была здорова и не курила, не принимая никаких лекарств. Клиническое обследование выявило температуру 38,5 ° С, частоту пульса 120 ударов в минуту, артериальное давление 140/80 мм рт.ст., частоту дыхания 22 вдоха в минуту и насыщение кислородом 98% при дыхании окружающим воздухом. При аускультации легких выявляется двухосновный хрип На презентации в день 4 SARS-CoV-2 был обнаружен в образце мазка из носоглотки методом ПЦР с обратной транскриптазой в реальном времени. SARS-CoV-2 был снова обнаружен на 5-6 день в образцах из носоглотки, мокроты и кала, но не обнаруживался с 7 дня (рис. 1а ). С-реактивный белок в крови был повышен до 83,2 с нормальным количеством лимфоцитов (4,3 × 10 9 клеток на литр (диапазон от 4,0 × 10 9 до 12,0 × 10 9 клеток на литр)) и нейтрофилов (6,3 × 10 9 клеток на литр (диапазон от 2,0 × 10 9 до 8,0 × 10 9 × 10 9 клеток на литр)).
Других респираторных патогенов обнаружено не было. Ее лечением была внутривенная регидратация жидкости без дополнительной оксигенации. Антибиотики, стероиды или противовирусные препараты не вводились. Рентгенография грудной клетки показала би-базальные инфильтраты на 5-й день, которые очистились на 10-й день (Рис. 1b ). На 11-й день она была выписана в домашнюю изоляцию. Ее симптомы полностью исчезли к 13-му дню, и на 20-й день она оставалась здоровой, с постепенным увеличением SARS-CoV-2-связывающих IgM и IgG-антител в плазме с 7-го по 20-й день (рис. 1с и расширенные данные рис. 1 ). Пациент был зачислен через Платформу готовности к исследованиям Sentinel Travelers для исследования новых инфекционных заболеваний нового коронавируса (SETREP-ID-coV) и предоставил письменное информированное согласие перед началом исследования. Уход за пациентами и их исследование проводились в соответствии с руководящими принципами ведения истории болезни и Хельсинкской декларацией. Эксперименты проводились с одобрениями этики HREC / 17 / MH / 53, HREC / 15 / MonH / 64 / 2016.196 и UoM # 1442952.1 / # 1443389.4.
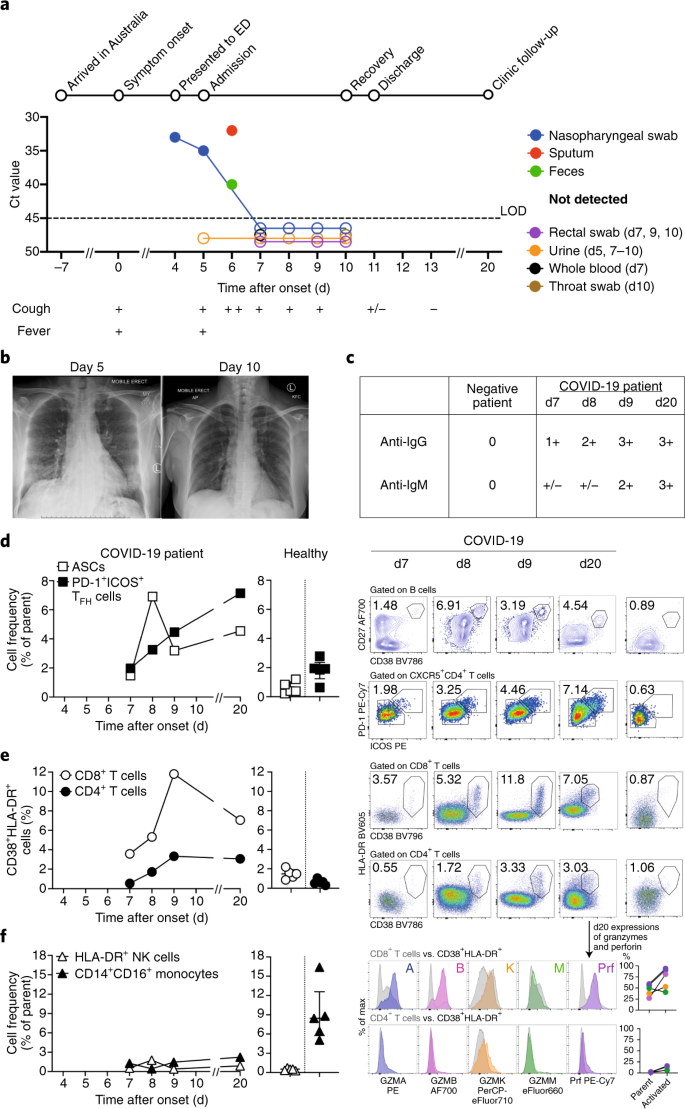
Рис. 1: Появление иммунных ответов при нетяжелых симптомах COVID-19.
Рисунок 1
a , Хронология COVID-19, показывающая обнаружение SARS-CoV-2 в мокроте, носоглоточных аспиратах и кале, но не в моче, ректальном мазке или цельной крови. SARS-CoV-2 определяли количественно с помощью rRT-PCR; порог цикла (Ct) показан. Более высокое значение Ct означает более низкую вирусную нагрузку. Пунктирная горизонтальная линия обозначает порог предела обнаружения (LOD) (Ct = 45). Открытые круги, необнаружимые SARS-CoV-2. б - рентгенограммы переднезадней грудной клетки на 5 и 10 дни после появления симптомов, показывающие радиологическое улучшение от госпитализации до выписки. c. Окрашивание иммунофлуоресцентными антителами, повторенное дважды в двух экземплярах, для выявления IgG и IgM, связанных с клетками Vero, инфицированными SARS-CoV-2, с оценкой в плазме (разбавленной 1:20), полученной в дни 7-9 и 20 после появления симптомов. d - f , частота (левый набор графиков) CD27 hi CD38 hi ASCs (gated на CD3 - CD19 + лимфоцитах) и активированных клеток ICOS + PD-1 + T FH (gated на CD4 + CXCR5 + лимфоцитах) ( d ), активированные CD38 + HLA-DR + CD8 + или CD4 + T-клетки ( e ) и CD14 + CD16 + моноциты и активированные HLA-DR + природные киллеры (NK) (стробированные на клетках CD3 - CD14 - CD56 + ) ( f ) выявляется с помощью проточной цитометрии крови, собранной в дни 7–9 и 20 после появления симптомов у пациента и у здоровых доноров ( n = 5; медиана с межквартильным диапазоном); примеры стробирования справа. Справа внизу гистограммы и линейные графики, окрашивание гранзима A (GZMA (A)), гранзима B (GZMB (B)), гранзима K (GZMK (K)), гранзима M (GZMM (M)) и перфорина (Prf) в родительские CD8 + и CD4 + T-клетки и активированные CD38 + HLA-DR + CD8 + и CD4 + T-клетки. Стробирование и экспериментальные подробности в расширенных данных Рис. 3 .
Источник данных
Изображение в полном размере
Мы проанализировали кинетику и широту иммунных реакций, связанных с клиническим разрешением COVID-19. Поскольку ASC являются ключом для быстрого производства антител после инфицирования вирусом Эбола 1 , 2 и инфицирования и вакцинации против вируса гриппа 2 , 3 , и активированные циркулирующие клетки T FH (клетки cT FH ) одновременно индуцируются после вакцинации против вируса гриппа 3 мы определили частоту ответов клеток CD3 - CD19 + CD27 hi CD38 hi ASC и CD4 + CXCR5 + ICOS + PD-1 + cT FH до симптоматического выздоровления. ASC появились в крови во время вирусного клиренса (день 7; 1,48%) и достигли пика на день 8 (6,91%). Появление клеток cT FH происходило одновременно в крови в день 7 (1,98%), увеличиваясь в день 8 (3,25%) и день 9 (4,46%) (рис. 1d ). Пик как ASCs, так и cT FH клеток был заметно выше у пациента с COVID-19, чем у здоровых участников контроля (0,61% ± 0,40% и 1,83% ± 0,77% соответственно (среднее значение ± sd); n = 5). Как ASCs, так и cT FH клетки заметно присутствовали во время реконвалесценции (день 20) (4,54% и 7,14% соответственно; рис. 1d ). Таким образом, наше исследование предоставляет данные о рекрутировании как ASCs, так и cT FH клеток в кровь этой пациентки, когда она еще была нездорова и за 3 дня до исчезновения симптомов.
Поскольку коэкспрессия CD38 и HLA-DR является ключевым фенотипом активации CD8 + Т-клеток в ответ на вирусные инфекции, мы проанализировали коэкспрессию CD38 и HLA-DR. Согласно сообщениям о лихорадке Эбола 1 и 4 , коэкспрессия CD38 и HLA-DR на CD8 + Т-клетках (оцениваемая как частота CD38 + HLA-DR + CD8 + Т-клеток) быстро увеличилась у этого пациента с 7 дня (3,57%) к 8-му дню (5,32%) и 9-му дню (11,8%), затем снизились на 20-й день (7,05%) (рис. 1д ). Кроме того, частота CD38 + HLA-DR + CD8 + T-клеток была намного выше у этого пациента, чем у здоровых людей (1,47% ± 0,50%; n = 5). CD38 + HLA-DR + T-клетки были также недавно зарегистрированы у пациента с COVID-19 в один момент времени 5 . Точно так же коэкспрессия CD38 и HLA-DR на CD4 + T-клетках (оцениваемая как частота CD38 + HLA-DR + CD4 + T-клеток) увеличилась между 7-м днем (0,55%) и 9-м днем (3,33%) в этом пациент, относительно здоровых доноров (0,63% ± 0,28%; n = 5), хотя и на более низких уровнях, чем уровень CD8 + Т-клеток. CD38 + HLA-DR + T-клетки, особенно CD8 + T-клетки, продуцировали большее количество гранзимов A и B и перфорина (на ~ 34–54% выше), чем их родительские клетки (CD8 + или CD4 + популяции; рис. 1e ) , Таким образом, появление и быстрое увеличение активированных CD38 + HLA-DR + T-клеток, особенно CD8 + T-клеток, на 7-9 день предшествовало разрешению симптомов. Подробная информация о воспроизводимости данных содержится в отчете о биологических науках.
Анализ моноцитов CD16 + CD14 + , которые связаны с иммунопатологией, показал более низкие частоты моноцитов CD16 + CD14 + в крови этого пациента на 7, 8 и 9 дни (1,29%, 0,43% и 1,47% соответственно), чем в у здоровых контрольных доноров (9,03 ± 4,39%; n = 5) (рис. 1f ), что, возможно, свидетельствует об оттоке моноцитов CD16 + CD14 + из крови в участок инфекции. Различий в активированных клетках-киллерах HLA-DR + CD3 - CD56 + не обнаружено.
Поскольку провоспалительные цитокины и хемокины являются предикторами тяжелых клинических исходов гриппа 6 , мы количественно оценили 17 провоспалительных цитокинов и хемокинов в плазме. Мы обнаружили низкие уровни хемокина МСР-1 (CCL2) в плазме пациента (расширенные данные, рис. 2а ), хотя это было сопоставимо с результатами, полученными для здоровых доноров (22,15 ± 13,81; n = 5), пациентов, инфицированных гриппом А вирус или грипп B, оцененный в дни 7–9 (33,85 ± 30,12; n = 5), и пациент, инфицированный коронавирусом человека HCoV-229e (40,56). Таким образом, в отличие от тяжелого птичьего гриппа H7N9, у которого были повышенные цитокины IL-6, IL-8, IL-10, MIP-1β и IFN-γ 6 , у этого пациента с COVID- были обнаружены минимальные провоспалительные цитокины и хемокины. 19, даже когда она была симптоматической в дни 7-9.
Поскольку однонуклеотидный полиморфизм rs12252-C / C в гене IFITM3 (который кодирует интерферон-индуцированный трансмембранный белок 3) связан с тяжелым гриппом 6 , 7 , мы проанализировали IFITM3 -rs12252 у пациента с COVID-19 и обнаружили « риск ' вариант IFITM3 -rs12252-C / C (расширенные данные, рис. 2b ). Поскольку распространенность IFITM3 -rs12252-C / C в китайском населении составляет 26,5% (проект «1000 геномов») 6 , дальнейшее исследование аллеля IFITM3 -rs12252-C / C в более крупных когортах людей с COVID-19 заслуживает внимания ,
В совокупности наше исследование дает новый вклад в понимание широты и кинетики иммунных реакций во время несерьезного случая COVID-19. Этот пациент не испытывал осложнений дыхательной недостаточности или острого респираторного дистресс-синдрома, не нуждался в дополнительной оксигенации и был выписан в течение недели после госпитализации в соответствии с нетяжелым, но симптоматическим заболеванием. Мы представили данные о наборе популяций иммунных клеток (ASC, T FH- клеток и активированных CD4 + и CD8 + T-клеток) вместе с антителами, связывающими SARS-CoV-2 IgM и IgG, в крови пациента до разрешения симптомы. Мы предлагаем, чтобы эти иммунные параметры были охарактеризованы у более крупных групп людей с COVID-19 с различной степенью тяжести заболевания, чтобы определить, можно ли их использовать для прогнозирования исхода заболевания и оценки новых вмешательств, которые могут минимизировать тяжесть и / или информировать кандидатов о защитной вакцине. Кроме того, наше исследование показывает, что устойчивые многофакторные иммунные ответы могут быть вызваны вновь появившимся вирусом SARS-CoV-2, и, подобно птичьему заболеванию H7N9 8 , ранние адаптивные иммунные ответы могут коррелировать с лучшими клиническими исходами.
Источник: nature.com













